用于精確定量控制注入患者體內(nèi)的液體,與貯液裝置和輸液管路配套使用的輸液泵�����,在我國屬于第二類醫(yī)療器械注冊產(chǎn)品�����,其分類編碼為14-02-01。本文為大家介紹輸液泵產(chǎn)品技術(shù)要求及醫(yī)療器械注冊審查要點���。
引言:用于精確定量控制注入患者體內(nèi)的液體�,與貯液裝置和輸液管路配套使用的輸液泵���,在我國屬于第二類醫(yī)療器械注冊產(chǎn)品,其分類編碼為14-02-01���。本文為大家介紹輸液泵產(chǎn)品技術(shù)要求及醫(yī)療器械注冊審查要點�。
一�����、輸液泵注冊單元劃分的原則
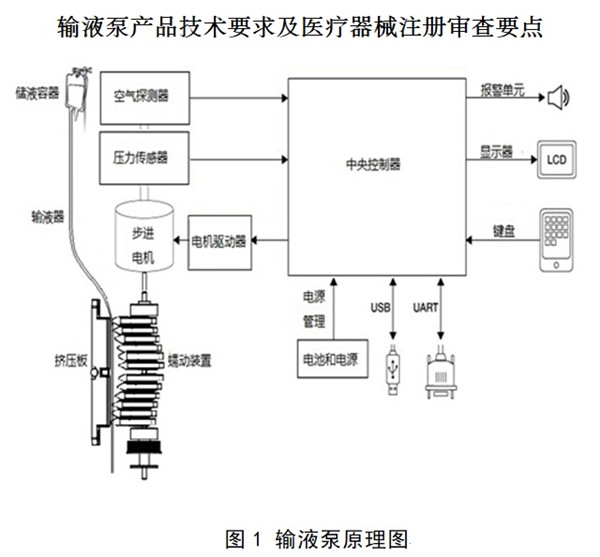
輸液泵主要由控制系統(tǒng)��、電機驅(qū)動單元���、蠕動擠壓機構(gòu)���、檢測裝置、報警裝置、輸入及顯示裝置����、殼體及其支撐結(jié)構(gòu)、軟件組件組成�����,與輸液器配套����,不接觸輸注液體,供醫(yī)院以可調(diào)節(jié)的方式為患者靜脈輸注藥液使用����。
輸液泵的醫(yī)療器械注冊單元原則上可按工作原理、設計��、技術(shù)參數(shù)���、附加輔助功能等不同分為若干型號���。
不同的電擊防護類型應作為不同注冊單元進行注冊。如電擊防護類型分別為I類��、II類輸液泵,應按照兩個注冊單元進行注冊���。
預期用途相同����,性能指標相近����,技術(shù)結(jié)構(gòu)基本相同的派生系列產(chǎn)品可以劃為同一注冊單元。例如帶藥物庫輸液泵和非帶藥物庫輸液泵可以劃為同一注冊單元��。
二���、輸液泵注冊產(chǎn)品工作原理
本輸液泵產(chǎn)品是根據(jù)GB 9706.224—2021《醫(yī)用電氣設備 第2—24部分:輸液泵和輸液控制器的基本安全和基本性能專用要求》標準中定義的輸液泵,請申請人根據(jù)申報產(chǎn)品具體描述產(chǎn)品的工作原理�����。預期通過泵產(chǎn)生的正壓來控制流入患者體內(nèi)的液體流量的ME設備�����。
在輸液泵運行過程中�����,管路壓力檢測傳感器、空氣傳感器�、滴數(shù)傳感器(如有)、溫度傳感器(如有)和電機轉(zhuǎn)速傳感器等持續(xù)監(jiān)測輸液泵的運轉(zhuǎn)狀態(tài)�,當異常情況出現(xiàn)時,輸液泵及時報警停機��。
三���、輸液泵產(chǎn)品技術(shù)要求
醫(yī)療器械注冊申請人應按照《醫(yī)療器械產(chǎn)品技術(shù)要求編寫指導原則》編寫產(chǎn)品技術(shù)要求����,結(jié)合申報產(chǎn)品的特點設置條款���。
輸液泵產(chǎn)品的主要技術(shù)性能指標應至少包括下列內(nèi)容�����,其中準確度的測試應同時在產(chǎn)品宣稱的可調(diào)范圍的極限值下進行:
3.1.1應明確產(chǎn)品輸液模式種類����。
3.1.2應明確輸液速度的可調(diào)范圍�����、步進及誤差。
3.1.3應明確輸液量的可調(diào)范圍�、步進及誤差。
3.1.4應明確KVO速度及誤差�。
3.1.5應明確(BOLUS或丸劑量)速度及誤差。
3.1.6應明確快注���、快排速度及誤差(如有)�����。
3.1.7應明確滴速精度及誤差(如有)�����。
3.1.8應明確加溫器加溫溫度范圍及誤差(如有)。
3.1.9應明確產(chǎn)品實時顯示的輸液量信息�����。
3.1.10應明確報警功能(應至少包含GB 9706.224及YY 9706.108中關(guān)于報警的要求�,如有其他報警功能,也應明確)���。
3.1.11設備產(chǎn)生的最大輸液壓力和阻塞報警閾值(壓力)的說明�。
3.1.12設備運行在最小速度和中速以及最小和最大可選阻塞報警閾值(壓力)時,阻塞報警觸發(fā)所需的最長時間����。
3.1.13設備運行在中速并且達到最小和最大阻塞報警閡值(壓力)時,產(chǎn)生的丸劑量的說明�����。
3.1.14當設備使用內(nèi)部電源供電并以中速運行時��,通常的運行時間��。
3.1.15單一故障狀態(tài)下可能傳輸?shù)淖畲笕萘俊?/p>
3.1.16無線功能及無線接口工作頻率(如有)���。
3.1.17推薦使用輸注管路的清單�,明確生產(chǎn)廠家����、規(guī)格型號。
注:注冊檢測時���,可選擇一種輸注管路進行全項檢測����。其他輸注管路可由檢測所或生產(chǎn)企業(yè)進行驗證,驗證至少包含流速試驗���。
3.1.18外觀要求�����。
3.1.19電氣安全
應符合GB 9706.1—2020《醫(yī)用電氣設備 第1部分:基本安全和基本性能的通用要求》�、GB 9706.224—2021《醫(yī)用電氣設備 第2-24部分:輸液泵和輸液控制器的基本安全和基本性能專用要求》���、YY9706.108—2021《醫(yī)用電氣設備 第1-8部分:基本安全和基本性能的通用要求 并列標準:通用要求,醫(yī)用電氣設備和醫(yī)用電氣系統(tǒng)中報警系統(tǒng)的測試和指南》標準的要求�����。
3.1.20電磁兼容性
應符合YY9706.102《醫(yī)用電氣設備 第1-2部分:基本安全和基本性能的通用要求 并列標準:電磁兼容 要求和試驗》及GB 9706.224—2021《醫(yī)用電氣設備 第2-24部分:輸液泵和輸液控制器的基本安全和基本性能專用要求》標準中生命支持設備或系統(tǒng)的要求����。
如有輸液泵產(chǎn)品技術(shù)要求及醫(yī)療器械注冊咨詢服務需求�,歡迎您隨時方便與杭州證標客醫(yī)藥技術(shù)咨詢有限公司聯(lián)絡�,聯(lián)系人:葉工,電話:18058734169���,微信同�����。